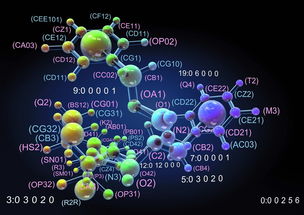
分子结构生物制药科技 生物科技领域的精准革命

在21世纪的生物科技浪潮中,分子结构生物制药科技正以前所未有的精准度和效率,引领着医药研发与生产的深刻变革。这一技术深度融合了结构生物学、计算科学、基因工程与药物化学,通过解析并利用生物大分子的三维结构信息,实现了从“盲筛”到“理性设计”的跨越,为人类对抗复杂疾病提供了全新武器。
一、核心技术:从结构解析到药物设计
分子结构生物制药的核心在于对靶点蛋白(如受体、酶)及其与潜在药物分子相互作用方式的精确理解。借助X射线晶体学、冷冻电镜(Cryo-EM)和核磁共振(NMR)等技术,科学家能够绘制出靶点蛋白在原子级别的三维结构图。通过计算机辅助药物设计(CADD),特别是基于结构的药物设计(SBDD),研究人员可以像“拼装钥匙”一样,虚拟筛选或从头设计出能精准结合靶点活性位点的小分子或大分子(如抗体、多肽),从而高效调控疾病相关的生物通路。
二、应用突破:重塑治疗范式
1. 抗体药物与蛋白工程:基于对抗原-抗体结合界面的结构洞察,科学家能够优化抗体的亲和力、特异性与稳定性。例如,针对癌症免疫检查点(如PD-1/PD-L1)的抗体药物,通过阻断特定蛋白相互作用,成功激活了患者自身的抗肿瘤免疫。
2. 小分子靶向药:在肿瘤治疗领域,针对致癌驱动基因突变(如EGFR、ALK)设计的小分子抑制剂,能精准抑制异常活跃的激酶活性,显著提升疗效并降低副作用。
3. 新兴疗法:结构生物学助力了更复杂疗法的开发,如PROTAC(蛋白降解靶向嵌合体)技术,它利用小分子将致病蛋白“标记”给细胞内的降解系统,从而彻底清除靶点,为“不可成药”靶点提供了新策略。
三、挑战与未来前景
尽管前景广阔,该领域仍面临挑战:许多靶点蛋白结构动态且复杂,难以解析;药物设计需兼顾效力、选择性、药代动力学等多重属性;研发成本高昂。随着人工智能与机器学习的深度介入,尤其是AlphaFold等工具预测蛋白结构能力的突破,药物发现流程将进一步加速。个性化医疗将更依赖于对患者特定基因变异所导致蛋白结构差异的理解,实现真正“量体裁衣”式的治疗。
****
分子结构生物制药科技不仅是生物科技皇冠上的明珠,更是推动现代医学进入精准时代的核心引擎。它深刻诠释了“结构决定功能”的生物学真理,并将继续通过持续的技术融合与创新,为攻克癌症、自身免疫疾病、神经退行性疾病等重大健康挑战开辟充满希望的路径。
如若转载,请注明出处:http://www.rzjyjc.com/product/291.html
更新时间:2026-05-26 12:28:02